
1 .Sifat Koligatif Larutan _ c. Kenaikkan Titik Didih dan Penurunan Titik Beku Larutan YouTube
Sifat koligatif larutan itu ada empat macam, yaitu p enurunan tekanan uap (Δ P), penurunan titik beku (Δ Tf), kenaikan titik didih (Δ Tb), dan tekanan osmotik (π). Kenapa ya simbol dari keempat sifat koligatif larutan itu beda-beda? Terus, arti dari setiap simbolnya itu apa, sih? Eits! tenang, guys. Misteri itu akan kamu pecahkan, kok!

Rumus titik beku larutan
T f = titik beku larutan. Penurunan titik beku larutan elektrolit. Rumus penurunan titik beku larutan elektrolit sebagai berikut: ΔT f = K f. m . {1 + (n - 1) α} Keterangan: n = jumlah ion; α = derajat ionisasi; Contoh soal dan pembahasan. Contoh soal 1. Sebanyak 2,4 gram urea (Mr = 60) dilarutkan dalam 50 gram air.

Praktikum Penurunan Titik Beku Pada Pembuatan Es Krim II Sifat Koligatif Larutan YouTube
Penurunan titik beku adalah selisih antara titik beku pelarut dengan titik beku larutan. Penurunan titik beku ini termasuk salah satu sifat koligatif larutan. Dalam perhitungan kimia, penurunan titik beku disimbolkan dengan ΔT f (f berasal dari kata freeze) atau ΔT b . Peristiwa penurunan titik beku ini sering diterapkan pada negara-negara.
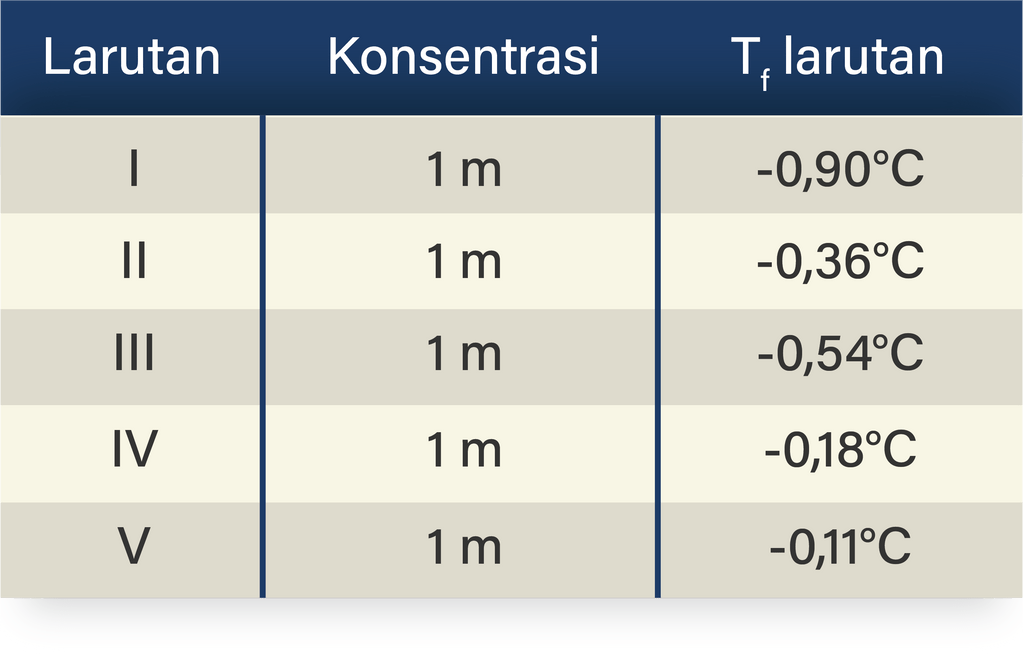
Berikut ini data titik beku beberapa larutan dalam...
Titik beku larutan lebih rendah daripada titik beku pelarut murni. Hal ini disebabkan zat pelarutnya harus membeku terlebih dahulu, baru zat terlarutnya. Jadi larutan akan membeku lebih lama daripada pelarut. Setiap larutan memiliki titik beku yang berbeda. Titik beku suatu cairan akan berubah jika tekanan uap berubah, biasanya diakibatkan oleh.

Contoh Soal Titik Beku Larutan (Sifat Koligatif Larutan Elektrolit) YouTube
Larutan yang dihasilkan atau campuran padatan-padatan tersebut memiliki titik beku lebih rendah daripada pelarut atau padatan murninya. Fenomena inilah yang menyebabkan air laut , (campuran garam [dan lainnya] dalam air) tetap cair pada suhu di bawah 0 °C (32 °F), titik beku air murni.

Berikut data titik beku (Tf) beberapa larutan elektrolit
Titik beku larutan = 0 °C - 18,6 °C = -18,6 °C. Titik beku larutan 64 gram naftalena dalam 100 gram benzena adalah 2,91 °C. Jika titik beku benzena 5,46°C dan tetapan titik beku molal benzena 5,1 °C, maka tentukan massa molekul relatif naftalena! Jawab: ΔTf = m × Kf ΔTf = massa benzena/Mr x 1.000/p x Kf

Penurunan Titik Beku Larutan Definisi Dan Penyebabnya Reverasite
Video ini membahas materi kimia Kelas XII MIPA yaituTitik Beku Larutan Non Elektrolit. Video ini dibuat untuk membantu siswa/i agar lebih memahami materi pel.

Apa yang dimaksud dengan penurunan titik beku 2021
Pengertian dan Rumus Penurunan Titik Beku Menurut Rananda Vinsiah dalam Fenomena Sifat Koligatif Larutan Kimia Kelas XII (2020, hlm. 19), titik beku merupakan kondisi ketika tekanan uap suatu cairan sama dengan tekanan padatannya. Pada kondisi seperti itu, cairan akan mulai membeku. Seandainya ada suatu zat terlarut yang dicampurkan ke pelarut murni, akan tercipta larutan baru.
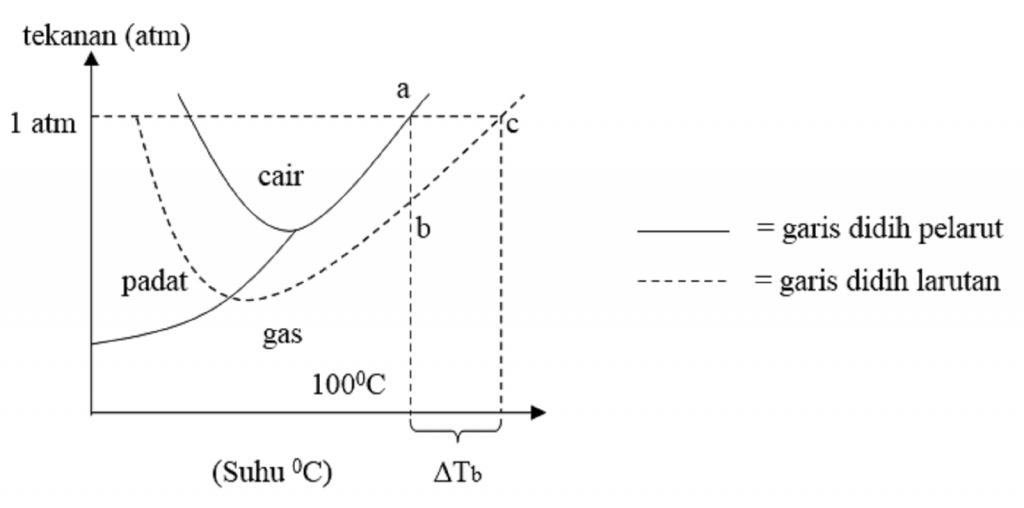
Sifat Koligatif Larutan Kenaikan Titik Didih Dan Penurunan Titik Beku Reverasite
3. Penurunan titik beku Titik beku adalah suhu pada tekanan tertentu yang menyebabkan perubahan zat dari cair ke wujud padat. Jika zat pelarut (air) dicampur dengan zat terlarut dan didinginkan hingga 0⁰C, ternyata larutan tersebut tidak membeku. Agar bisa beku, maka larutan harus didinginkan dengan suhu yang lebih rendah lagi.

Data percobaan penurunan titik beku Larutan Konsentrasi
Titik beku. inggit prakasa. Apabila suatu zat dilarutkan dalam suatu pelarut, maka sifat larutan itu berbeda dari sifat pelarut murni. Contohnya, larutan urea yang berbeda sifat dengan air murni biasa. Sifat-sifat larutan yang ada, seperti rasa, warna, pH, dan kekentalan bergantung pada jenis dan konsentrasi zat yang terlarut.
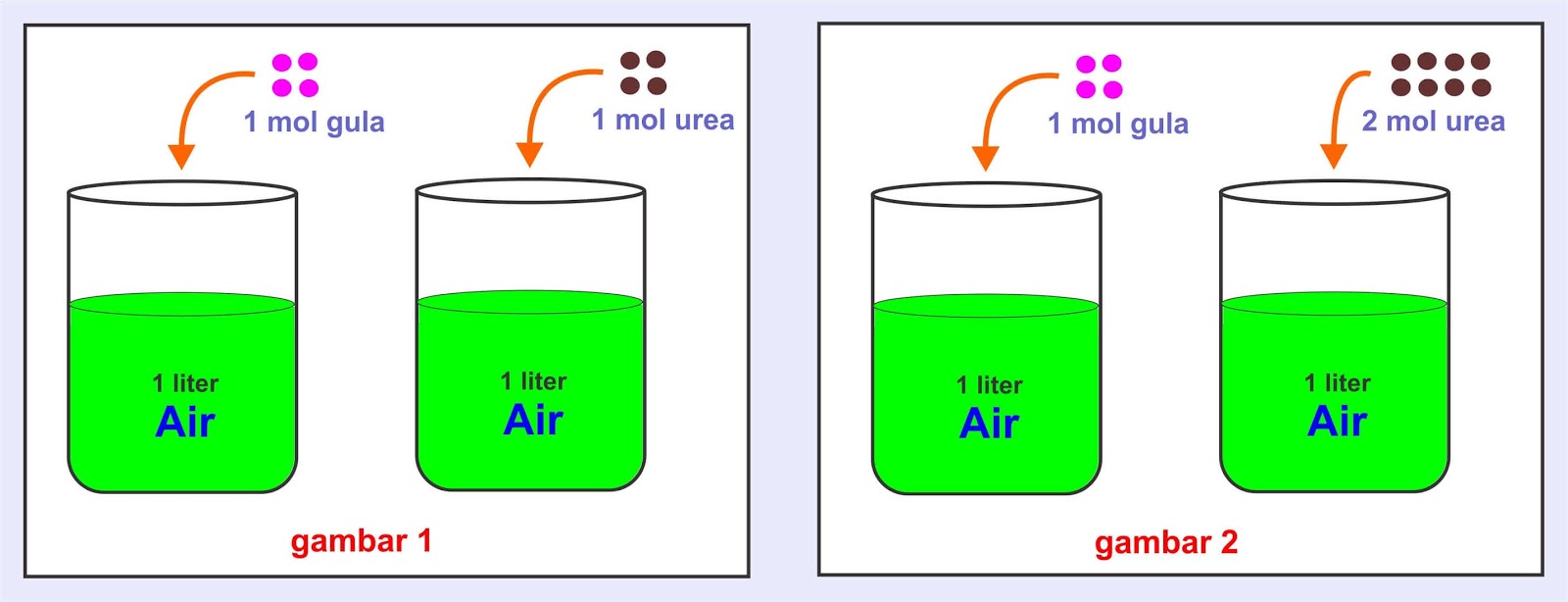
Modul I Sifat Koligatif Larutan Penurunan Titik Beku Larutan Mobile
Demikian pula pada penurunan titik beku larutan, tekanan uap larutan juga lebih rendah daripada tekanan uap pelarut murni. Sehingga agar larutan membeku, harus didinginkan ke suhu yang lebih rendah akibatnya titik beku larutan lebih rendah dari titik beku pelarut murni.

Contoh Soal Titik Beku Larutan (Sifat Koligatif Larutan Elektrolit) YouTube
Penurunan titik beku adalah salah satu sifat koligatif larutan yang dipengaruhi oleh beberapa faktor. Faktor-faktor yang mempengaruhi penurunan titik beku meliputi: Konsentrasi Partikel Terlarut: Semakin tinggi konsentrasi partikel terlarut dalam larutan, semakin besar penurunan titik beku yang terjadi. Ini berarti larutan dengan konsentrasi.

Contoh Soal Perbandingan Penurunan Titik Beku (Sifat Koligatif Larutan Elektrolit) YouTube
Misalnya, titik beku normal air adalah 0 o C. Akan tetapi, dengan adanya zat terlarut pada suhu 0 o C, air bisa mejadi belum membeku. Selisih titik beku pelarut (Tf o) dengan titik beku larutan (Tf) yang kemudian disebut penurunan titik beku (ΔTf). Berikut rumus penurunan titik beku: ΔTf = Tf° - Tf

Penurunan Titik Beku Larutan Dan Contoh Soal Faktasantuy Com My XXX Hot Girl
Titik beku larutan = 0 °C - 18,6 °C = -18,6 °C. 2. Diketahui Mr Urea (CO(NH2)2) = 60 g/mol, Kf air = 1,86 0 C/m, dan tekanan uap pelarut air pada suhu 25 0 C sebesar 23,75 mmHg, dan tekanan uap larutan urea pada 25 0 C sebesar 22,56 mmHg. Titik beku larutan urea tersebut adalah…

Larutan yang memiliki titik beku paling rendah adalah.
4. Jenis zat terlarut juga dapat mempengaruhi titik beku larutan, dengan zat terlarut yang lebih berat memiliki efek yang lebih besar pada titik beku larutan. 5. Kompleks yang terbentuk dari zat terlarut dapat membentuk lapisan yang melindungi molekul cairan dari pembekuan dan menyebabkan titik beku larutan turun. 6.

Perhatikan diagram PT air, larutan urea 0,1 m dan NaC...
Titik beku. Titik beku adalah suatu kondisi suhu saat zat cair berubah wujud menjadi padat. Adapun titik beku besarnya sama dengan titik lebur yakni 0°C. Titik lebur. Titik lebur atau titik leleh adalah suatu kondisi suhu saat benda padat meleleh menjadi cair. Sementara itu, titik lebur suatu zat dipengaruhi oleh: Tekanan